
Ермил
7 год назад
Сколько углекислого газа (CO2) образуется при разложении 8,4 г MgCo3, ответ в дать в литрах
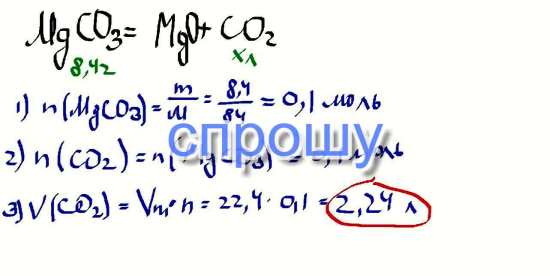
ОТВЕТЫ

Демидович
Jul 8, 2019
8,4 г х л
MgCO3 =gt; MgO + CO2
1 моль 1 моль
84 г/моль 22,4 л/моль
84 г 22,4 л
8,4/84=х/22,4
х=V(CO2) = 2,24 л
Ответ: 2,24 л
MgCO3 =gt; MgO + CO2
1 моль 1 моль
84 г/моль 22,4 л/моль
84 г 22,4 л
8,4/84=х/22,4
х=V(CO2) = 2,24 л
Ответ: 2,24 л
Очень простая задача
224
Смежные вопросы:
